中国疫苗国家监管体系或超国际标准 有利我国疫苗出口
2014年7月4日,世界卫生组织宣布,“中国疫苗国家监管体系达到或超过世卫组织按照国际标准运作的全部标准”。这是自2011年3月首次通过评估后,再次得到国际认证。
长期以来我国疫苗产品出口受国外注册等技术壁垒制约。由于国外对疫苗产品质量标准要求非常严格,加之企业的国际市场开拓能力不足,投入的资金和精力也不够,同时受药品注册法规限制,出口难度大,造成我国疫苗产品进出口贸易逆差过大,前瞻产业研究院《2014-2018年中国疫苗行业深度调研与投资战略规划分析报告》数据显示,2009-2013年我国疫苗进出口贸易逆差均在6亿美元以上,且逐年较快增长,到2013年已经达到30.93亿元。虽然国内有部分疫苗出口韩国、巴基斯坦以及WHO,但是量都很小,而且没有长期合同。
图表1:2009-2013年中国疫苗行业进出口贸易逆差及其增长情况(单位:万美元,%)
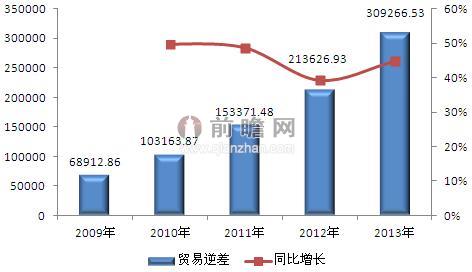
数据来源:前瞻产业研究院
之所以说通过WHO认证有利于我国疫苗产品出口是因为,与美国FDA和欧盟CMC认证相比,WHO认证体系固然看重疫苗的安全性和质量,但更侧重于疫苗的经济性,国内疫苗由于成本、价格较低,质量标准较高,能满足于发展中国家疫苗需求。
另外,近年来,随着我国疫苗技术水平的提高及国际贸易环境的改善,我国疫苗产品出口限制开始松动。2009年6月,国家税务总局和财政部发布了最新出口退税率调整通知,胰岛素、人用疫苗、血制品和抗生素等产品的出口退税率由原13%上调到15%,推动了疫苗的出口。
基于价格优势,我国人用疫苗在亚洲和非洲市场发展较快,主要出口市场是印度、巴基斯坦、韩国、马拉维和泰国,所占比重高达80%以上。2013年10月,成都生物制品研究所的乙脑疫苗成为首个通过WHO预认证的疫苗,被列入联合国采购清单。
不过,虽然前景看好,我国疫苗行业巨大的进出口贸易逆差仍是不可忽视的事实,发达国家的大门敲不开就意味着我国疫苗行业发展仍面临较大的挑战,而且从进出口贸易差可以看出,目前我国疫苗行业技术研发能力仍有待提高。
广告、内容合作请点这里:寻求合作
咨询·服务

