国家药监局:我国创新药械研发上市迎来爆发期【附我国创新药、创新医疗器械发展现状】

图源:摄图网
7月5日,国家药监局局长焦红在国务院新闻办公室召开的“权威部门话开局”系列主题新闻发布会上指出,近年来,国家药监局持续推进药品医疗器械审评审批制度改革,鼓励药品医疗器械创新的政策红利不断释放,药品医疗器械质量持续提升,药品研发创新活力不断提升,我国创新药械研发上市迎来爆发期。
中国创新药:新产品研发活跃,批准趋严
2020-2022年,中国批准创新药临床试验的数量有所增加,而上市批准数量则在2021年大幅上升后在2022年由于批准趋严而大幅下降。2022年,中国批准临床品种数量增加至1615件;项目上市18件,其中中药天然药物5件,化学药品9件,生物制品4件。
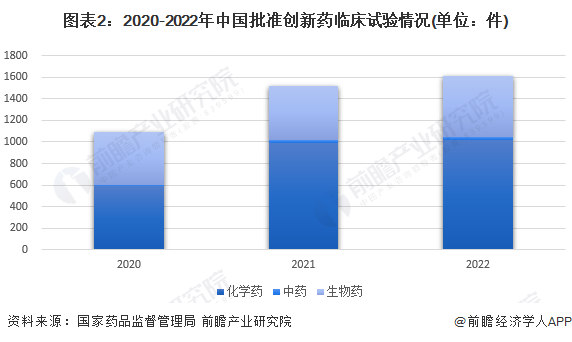
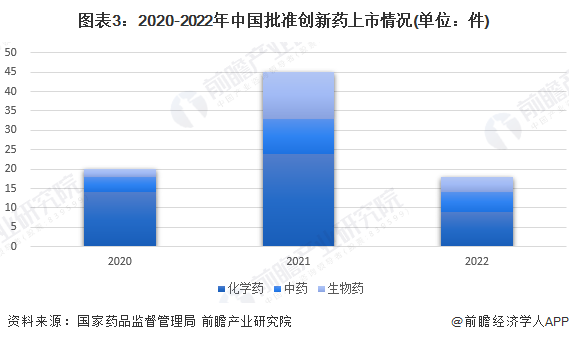
中国创新医疗器械:国内首创,技术处于国际领先水平
创新医疗器械是指申请人经过其主导的技术创新活动,在中国依法拥有产品核心技术发明专利权,或者依法通过受让取得在中国发明专利权或其使用权;或者核心技术发明专利的申请已由国务院专利行政部门公开。2014年以来,国家药监局通过构建创新医疗器械优先审评审批、绿色通道等措施,助力多项创新医疗器械和临床急需医疗器械快速获准上市,企业创新积极性高涨,产业发展迅速。
截止到2022年5月26日,经过我国药监局获批上市的创新医疗器械共有160个。从年份的获批情况来看,近年来获得我国药监局批准上市的创新医疗器械呈现波动上升态势;从2014年1个上升至2021年的35个。2022年1-5月,获得我国药监局批准上市的创新医疗器械有26个,与2020年持平。
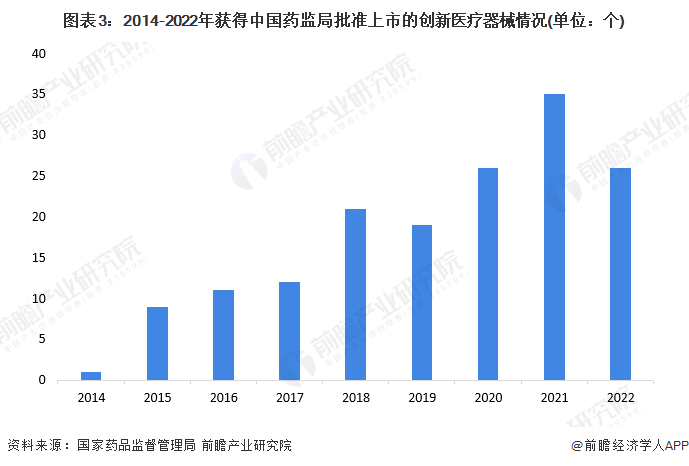
从地区的角度来看,获得我国批准上市的创新医疗器械95%隶属于本土地区。而隶属于境外企业的共有8个产品;来自于美敦力公司、NovoCure Ltd.、Edwards Lifesciences LLC、Abbott Vascular、Sequent Medical Inc.、W.L. Gore & Associates, Inc.等6家公司。

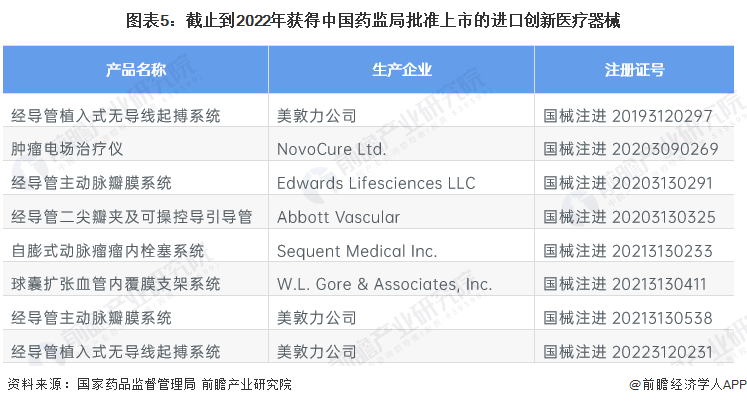
注:截止日期为2022年5月26日。
从省市的角度来看,获批上市的创新医疗器械产品多数来自于北京、上海、广东、江苏和浙江;分别为46个、28个、25个、23个、11个。
前瞻经济学人APP资讯组
更多本行业研究分析详见前瞻产业研究院《中国生物医药行业发展前景预测与投资战略规划分析报告》;《中国医疗器械行业市场前瞻与投资战略规划分析报告》。
同时前瞻产业研究院还提供 产业大数据、产业研究报告、产业规划、园区规划、产业招商、 产业图谱 、智慧招商系统、行业地位证明 、IPO咨询/募投可研 、IPO工作底稿 咨询等解决方案。在招股说明书、公司年度报告等任何公开信息披露中引用本篇文章内容,需要获取前 瞻产业研究院的正规授权。
更多深度行业分析尽在【前瞻经济学人APP】,还可以与500+经济学家/资深行业研究员交流互动。
广告、内容合作请点这里:寻求合作
咨询·服务

