谭蔚泓院士/刘尽尧研究员Angew:核酸适配体-多药偶联物自组装胶束增强PD-1疗效
作者|高分子科学前沿 来源|高分子科学前沿(ID:Polymer-science)
肿瘤细胞可以利用免疫检查点蛋白之间的相互作用实现免疫逃逸,基于抑制免疫检查点阻断策略的肿瘤免疫疗法已在多种晚期实体瘤相关的患者中获得了持久的反应。由于肿瘤的异质性及肿瘤微环境的复杂性,免疫检查点抑制剂治疗的总体有效率较低,仍有很多方面存在改进的空间。虽然传统化疗或放疗可以提高免疫检查点抑制剂疗法的响应率,但目前该类方法引起的免疫反应仍不能令人满意,这主要归因于抗原产生以及免疫抑制肿瘤微环境逆转不足等结果。当前,纳米药物虽然广泛用于免疫佐剂,但其面临的低载药量和靶向性差等问题,容易导致肿瘤组织中药物蓄积的不足。近日,上海交通大学分子医学研究院谭蔚泓院士和刘尽尧研究员报道了一种使用核酸适配体-多药物偶联物(ApMDC)纳米胶束作为肿瘤靶向的化疗制剂,通过诱导癌细胞的免疫原性死亡激发检查点抑制的抗肿瘤免疫应答。
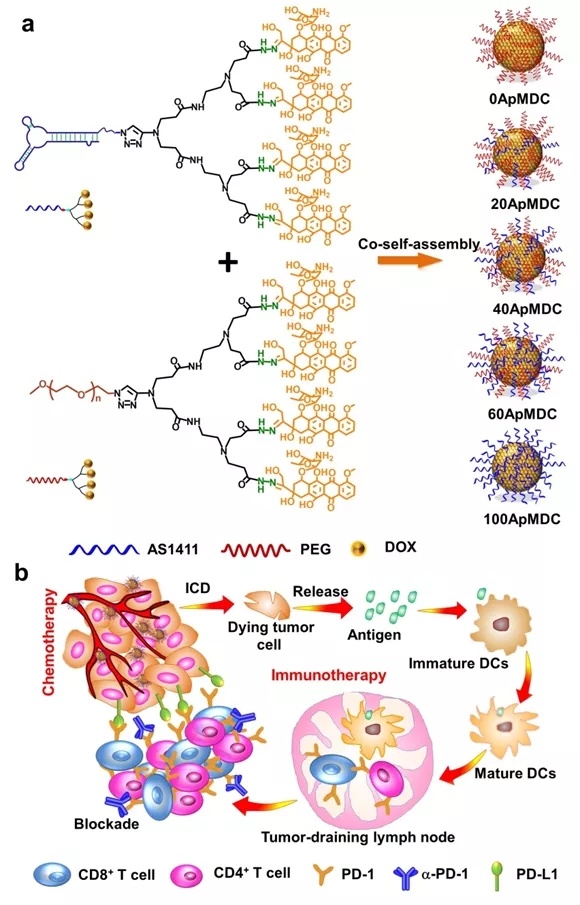
通过将亲水性核酸适配体与疏水性药物分子缀合得到两亲性大分子,该两亲性大分子在水溶液中自组装形成ApMDC纳米胶束。胶束表面的核酸适配体密度可以通过与PEG-多药偶联物类似物共组装进行调节,从而筛选出具有最优肿瘤靶向性的ApMDC纳米胶束。在此基础上,以免疫正常的4T1和H22荷瘤小鼠为动物模型,系统评估了ApMDC纳米胶束增强anti-PD1抗癌免疫应答的能力,验证了该策略的通用性以及ApMDC纳米胶束的治疗潜力。
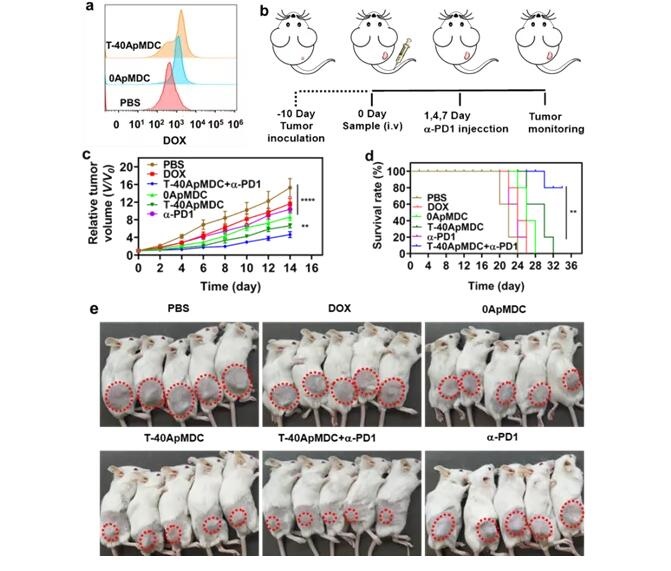
论文链接:
https://onlinelibrary.wiley.com/doi/10.1002/anie.202102631
编者按:本文转载自微信公众号:高分子科学前沿(ID:Polymer-science)
广告、内容合作请点这里:寻求合作
咨询·服务

