中山大学刘杰副教授团队在肿瘤微环境响应型纳米药物载体领域取得新进展
作者|老酒高分子 来源|高分子科技(ID:Polymer-China)
纳米药物递送系统(NDDSs)能够通过被动靶向效应聚集于肿瘤部位,同时具有缓释、靶向等诸多优点,是新型药物递送系统研究的热点。但是肿瘤区域的异质结构和独特的微环境形成了一系列生物屏障,例如高肿瘤间质流体压力(IFP)和致密的肿瘤细胞外基质(ECM),在很大程度上阻止了NDDSs深入肿瘤组织。研究发现,可以通过调节NDDSs的粒径、形状以及表面性质等来改善其肿瘤穿透和细胞摄取效率。提高肿瘤治疗效果的另一种方法是使用对具有肿瘤特异性刺激的NDDSs来控制药物释放,但是肿瘤微环境中常见内源性刺激水平含量比较低且分布不均匀,无法实现有效控制NDDSs的药物释放。所以改善NDDSs的低肿瘤穿透能力和不受控制的药物释放行为将极大提高其在临床上的应用。
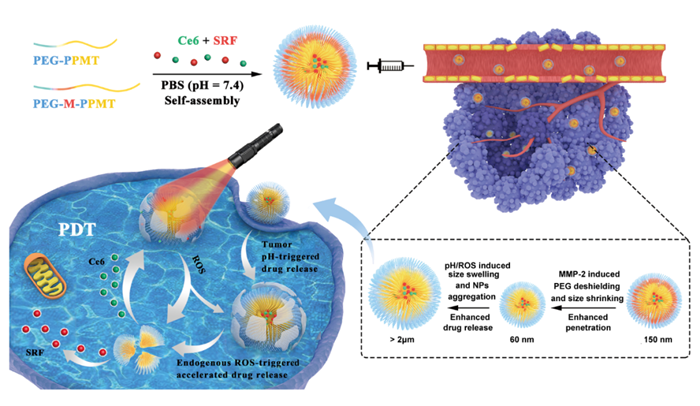
近年来,中山大学生物医学工程学院刘杰副教授课题组构建了一系列基于功能性聚酯的肿瘤酸性以及氧化还原响应的纳米药物递送载体(Materials Science & Engineering C, 2020, 111125, Journal of Materials Chemistry B, 2019,7, 651, ACS Applied Materials & Interfaces, 2017, 9: 30519)。在此基础上,该团队设计了一种新型的pH/ROS/MMP-2三重响应性PEG-M-PPMT纳米颗粒同时包载抗癌药物索拉非尼(SRF)和光敏剂(Ce6),实现了肿瘤部位高聚集、高穿透且具有级联放大释药功能的化疗/光动力学联合治疗。静脉给药后,PEG-M-PPMT纳米粒子可通过EPR效应聚集在肿瘤部位;随后肿瘤细胞外基质中过度表达的金属基质蛋白酶(MMP-2)可使该纳米粒子部分脱落PEG冠形成更小的颗粒并深入肿瘤组织;纳米粒子被肿瘤细胞摄取后,胞内的酸性介质和高ROS水平会引起纳米颗粒溶胀,加速药物释放,从而达到快速杀伤癌细胞的目的。更进一步,通过体外激光辐照光敏剂Ce6,可快速提高肿瘤细胞内活性氧浓度,进一步促进载体内药物的级联释放,最终实现高效的多重响应型肿瘤化疗和光动力一体化联合治疗。
该研究成果“Tumor microenvironment triple-responsive nanoparticles enable enhanced tumor penetration and synergetic chemo-photodynamic therapy”发表于生物材料权威期刊Biomaterials (DOI: 10.1016/j.biomaterials.2020.120574),中山大学生物医学工程学院硕士生舒曼和唐俊杰为论文的共同一作,刘杰副教授和耶鲁大学Zhaozhong Jiang研究员为本研究的共同通讯作者,中山大学生物医学工程学院为第一单位和主要完成单位。
该研究工作得到国家自然科学基金(51773231)、广东省自然科学基金(2016A030313315)和广东省传感技术与生物医学仪器重点实验室项目(2011A060901013)的资助。
原文链接:
https://doi.org/10.1016/j.biomaterials.2020.120574
编者按:本文转载自微信公众号:高分子科技(ID:Polymer-China)
广告、内容合作请点这里:寻求合作
咨询·服务

