Science评Nature子刊综述,共同解密新冠病毒致死原因,解析治疗新策略
作者|Hanson 来源|Hanson临床科研(ID:HClinicalResearch)
在我们的临床医生讨论群里,大家最痛心的就是本来病情已经有明显回复的患者却突然再次加重甚至死亡。新型冠状病毒(SARS-CoV-2)导致的疾病(COVID-19)患者就经常出现这种情况,包括我们非常敬重也是非常惋惜的李文亮医生。大家也一直有一点困惑不解,按理说体外膜氧合肺(ECMO)对于肺部疾病的青中年是非常有效的。是什么原因导致了这些患者最后竟然还是死去?
医生科学家也注意到了这个问题,2020年4月17日,Science报道了其发现,新冠病毒全面攻击人体的主要脏器(Science)。5月21日,新英格兰医学杂志(NEJM)报道了美国Brigham and Women’s Hospital的7例COVID-19尸体剖检结果,发现COVID-19患者表现出特征性的病理变化:血管内皮损伤、病毒进入细胞内及细胞膜结构的破坏。COVID-19患者微血管血栓发生率是H1N1患者的9倍(NEJM)。
与此同时,欧美儿科医生科学家也发现了COVID-19感染患儿出现了一系列前所未有的疾病综合征:新冠病毒感染后致死性“儿童多系统炎性综合征”,5月6日柳叶刀(Lancet)杂志报道了患儿出现发热、皮疹、眼睛发红、手脚肿胀和剧烈腹痛,部分患儿出现休克症状,没有咳嗽和呼吸急促,检查时发现患儿有淋巴结肿大和心肌损伤。部分患儿出现休克症状甚至死亡,但没有或较轻咳嗽和呼吸急促等呼吸道症状(Lancet)。
这些研究都共同指向:新冠病毒导致患者血管渗漏、凝血异常和过度炎症,是这些患者病情急剧恶化甚至死亡的关键。
基于此,Nat Rev Immuol综述了重症COVID-19的发病机制:血管渗漏、凝血异常和过度炎症。Teuwen等从细胞因子和免疫异常的角度阐述了血管内皮细胞损伤、通透性增加、凝血异常和炎症的病理生理学机制。该论文的题目是“COVID-19: the vasculature unleashed”,发表于2020年5月21日。因为该综述的意义非凡,Science于6月2日特发文章对该综述做出评论和解读。
重症COVID-19的发病机制
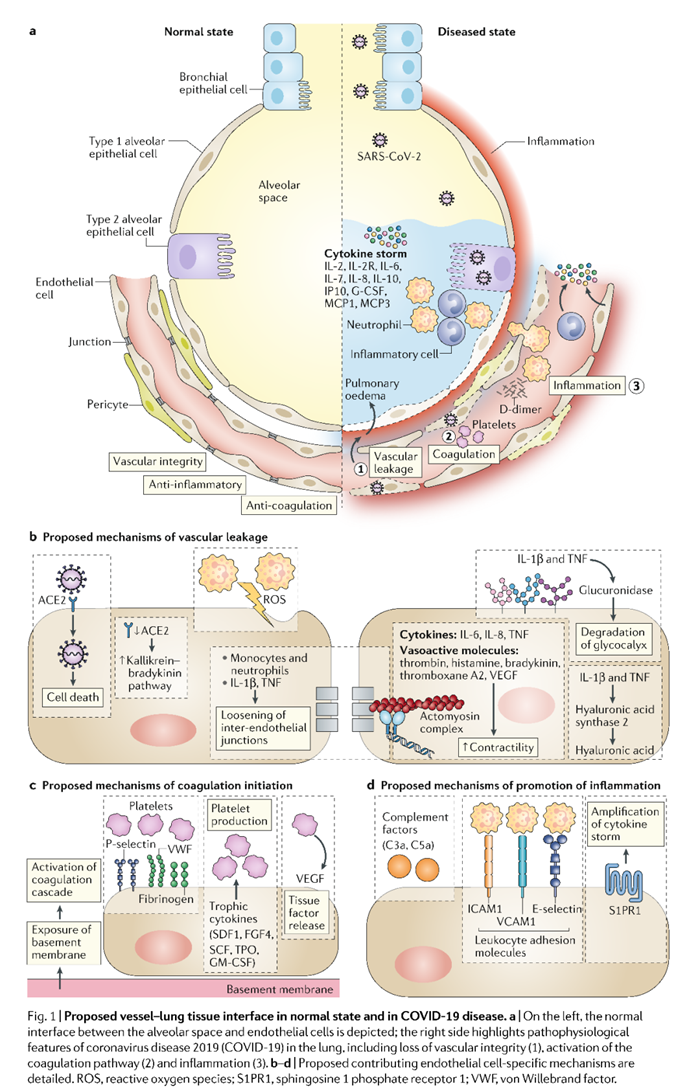
(来源:nature.com)
危重COVID-19患者的血管渗漏和肺水肿是由多种机制引起的(如上图所示)。首先,新冠病毒可以直接影响内皮细胞,因为在死者的多个器官中检测到了新冠病毒感染的内皮细胞。这时候表现出以内皮功能功能障碍、溶解和死亡为特征的广泛的内皮炎。其次,新冠病毒通过结合于ACE2受体进入细胞,这损害ACE2的活性。ACE2活性降低会间接激活激肽释放酶-缓激肽途径,从而增加血管通透性。第三,募集到肺部内皮细胞的活化中性粒细胞产生组织毒性介质,包括活性氧(ROS)。第四,免疫细胞、炎性细胞因子和血管活性分子破坏了内皮收缩力和内皮间连接。反过来,这将内皮分开,导致内皮间隙。最后,细胞因子IL-1β和TNF激活了葡糖醛酸糖苷酶,降解了糖萼,但也上调了透明质酸合酶2的水平,导致透明质酸在细胞外基质中的沉积增加,并促进了液体的滞留。
这些机制共同导致血管通透性增加和血管渗漏。
由此,炎症反应和免疫异常如细胞因子风暴等因素引起的肺血管内皮损伤和血管通透性增加会导致肺水肿、凝血异常和DIC;而在COVID-19患者中,感染本身可造成肺泡功能丧失,最终引起ARDS。感染和炎症互为因果,形成恶性循环,加速了疾病向重症进展、部分患者死亡。
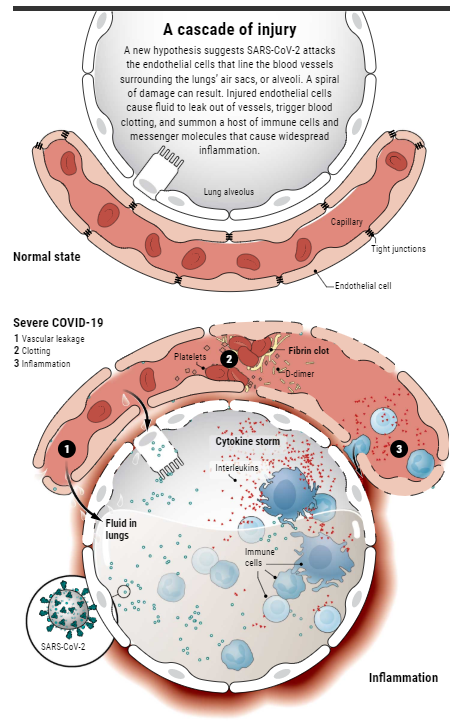
(血管内皮细胞正常状态和COVID-19感染后,来源:Sciencemag.org)
在这个过程中,本来作为人体防御手段的炎性应答却在致命的细胞因子风暴中失控地螺旋上升,活化的血管内皮在被损坏的同时也与免疫细胞一起释放大量炎性介质,导致广泛的毛细血管血栓形成。
COVID-19致死高危因素
该研究也解释了与COVID-19患者病死相关因素(老龄和基础疾病)与病死率增高相关的机制。COVID-19的危险因素(老年,肥胖,高血压和糖尿病)的特征都在于原有的血管功能障碍和内皮细胞代谢改变。
治疗危重COVID-19患者的新策略
基于上述研究,医生科学家也发起了一系列临床试验以通过干预微血管的血栓来达到治疗危重COVID-19患者的目的。比如,
1)靶向血管生成素2:基于血管生成素2的循环水平与ARDS患者肺水肿和死亡率增加相关的基本原理,一项临床试验(NCT04342897)正在探索靶向血管生成素2在COVID-19患者中的作用。2)bevacizumab:其他几项临床试验(NCT04344782,NCT04275414和NCT04305106)正在研究bevacizumab用于COVID-19患者。bevacizumab是一种与VEGF结合并抵消其血管通透作用的单克隆抗体。3)代谢干预:通过代谢干预使血管壁正常化可被视为另一种干预途径。例如,用靶向糖酵解途径的关键代谢酶的药物治疗的内皮细胞采取“正常化”表型,具有增强的血管完整性,减少的局部缺血和渗漏。
尽管针对危重COVID-19凝血异常的靶向治疗效果需要进一步验证,但内皮细胞和其他血管细胞发挥重要作用的可能性为将来的治疗机会铺平了道路。
小结:
本研究发现:
1)新冠病毒导致患者血管渗漏、凝血异常和过度炎症,是这些患者病情急剧恶化甚至死亡的关键。2)这一研究也解释了老龄和合并基础疾病的患者病死率高的机制。3)针对凝血异常的靶向治疗已经开始临床试验,期待这些新发现能来更精准的治疗和更好的临床预后。
原文链接:
https://www.nature.com/articles/s41577-020-0343-0
https://www.sciencemag.org/news/2020/06/blood-vessel-attack-could-trigger-coronavirus-fatal-second-phase
编者按:本文转载自微信公众号:Hanson临床科研(ID:HClinicalResearch),作者:Hanson
广告、内容合作请点这里:寻求合作
咨询·服务

