深圳罗兹曼研究院院长周国瑛团队发现hnRNPA2B1促进高尔基介导的病毒粒子胞外释放
作者|周国瑛课题组 来源|生命科学前沿(ID:advancedlifesci)
近日,深圳罗兹曼国际转化医学研究院“病毒与免疫”周国瑛教授团队在病毒学领域权威期刊Journal of Virology在线发表题为“hnRNPA2B1 associated with recruitment of RNA into exosomes plays a key role in HSV-1 release from infected cells”的论文,首次报道外秘体RNA转运蛋白hnRNPA2B1通过高尔基体介导的运输机制,既能促进外秘体的胞外释放,也能促进成熟的HSV-1病毒粒子的胞外释放,在病毒复制中起重要作用。
广泛存在于各种体液中的外秘体(exosomes)是一种能被机体内大多数细胞分泌的微小膜泡,具有脂质双层膜,直径大约为 30-150 nm。外泌体携带了参与细胞内信号转导的蛋白、miRNA、lncRNA、circRNA、mRNA以及其降解片段,形成细胞-细胞间信息传递系统,参与细胞活动的重要调控。
与外泌体产生相关的重要分子有:Ral、ARF6、PLD2、RAB家族。一些物质进入外泌体中是特异性的:如hnRNPA2B1,它能结合lncRNA或miRNA特异性的序列(GGAG/CCCU, EXO packaging motif),把它们带到外秘体中。周国瑛团队2018年首次报道了人工设计的靶向编码HSV-1主要调节蛋白ICP4的mRNA--miR401,miR401掺入hnRNPA2B1结合RNA的 EXO packaging motif。miR401被包装进入外泌体,纯化的含miR401的外泌体以剂量依赖性方式有效地阻断HSV-1复制(1)。之后,周国瑛团队又设计了包装进入外秘体的靶向编码CTLA-4的miRNA,该外泌体与携带PD-1的oHSV溶瘤病毒同时进行瘤内注射后,它可以增强oHSV在耐药肿瘤中的溶瘤活性(2)。
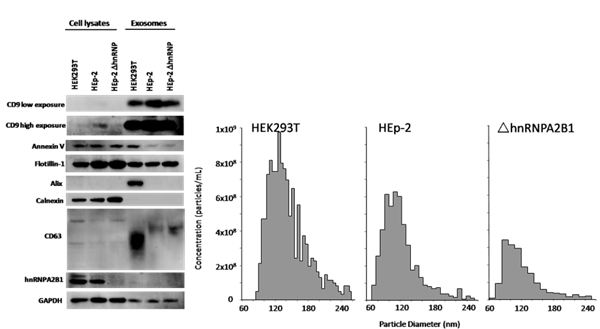
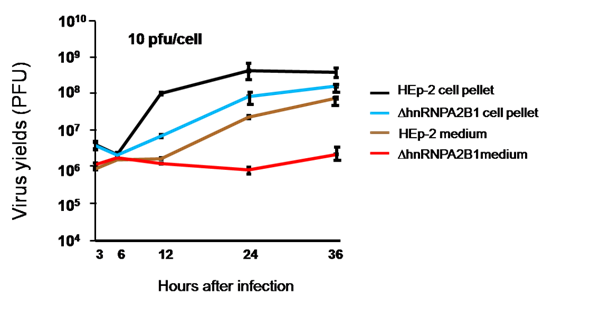
本次报道,周国瑛团队发现,纯化的HEp-2和HEK293T细胞外泌体中不含有hnRNPA2B1蛋白,尽管hnRNPA2B1的功能是结合lncRNA或miRNA特异性的序列(EXO packaging motif),把它们输送到外秘体中,但它自身并不进入外秘体内。将hnRNPA2B1从HEp-2中敲除后,细胞产生外秘体的数量减少一半以上,出乎意料的是,HSV-1病毒的复制在hnRNPA2B1敲除细胞中减低3倍以上,尤为重要的是,与HEp-2相比,hnRNPA2B1敲除后,它所释放到细胞外的病毒数量降低100倍以上。
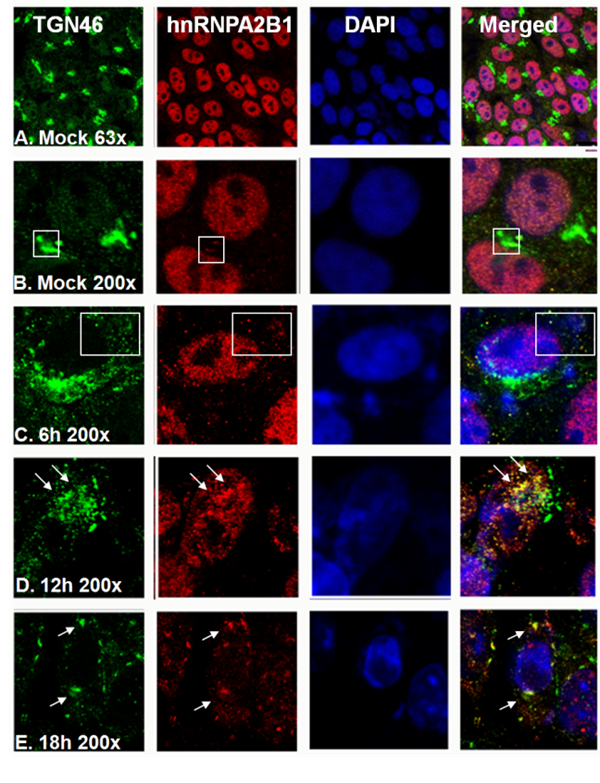
早期的研究表明,HSV通过两种不同的途径从感染细胞中释放(egress)(3,4),1) 通过感染的细胞与未感染的细胞直接接触向外扩散,2)通过高尔介导的转运从细胞膜包向胞外培养基的分泌。周国瑛团队的免疫荧光研究发现,hnRNPA2B1主要位于细胞核中,在未感染的细胞中,但在病毒感染的12-18小时,大量的hnRNPA2B1从细胞核涌出,快速转运到细胞质的高尔基体附近,研究预示,hnRNPA2B1正是在上述第二种病毒释放的途径中发挥了作用,而它也利用同样机制促进了外秘体的胞外释放。
周国瑛教授指导的周旭莎博士生(现广州医科大学)为论文的共同第一作者。该研究得到了深圳科创委孔雀计划的项目支持。

通讯作者简介
周国瑛,教授,博导,国家qian人计划特聘专家,2019年国际“抗病毒女科学家奖”获得者。中国科学院上海生物化学研究所博士,前芝加哥大学微生物系副教授; 深圳罗兹曼国际转化医学研究院创办人、院长;亦诺微医药CEO/CSO。在抗病毒感染与疱疹溶瘤病毒肿瘤免疫治疗研究领域潜心研究20多年,领导“病毒感染与天然免疫”、 “基因治疗的外泌体新药研发”两个基础理论研究课题,主持十三五国家重大新药创制、国家自然科学基金、广东省、广州市、深圳市的科研项目。周博士是疱疹靶向溶瘤病毒的国际发明人,2015年在深圳联合创办亦诺微医药,主领实体肿瘤的溶瘤病毒免疫与溶瘤双重治疗新药研发,首个产品进入中国和澳洲临床研究(Phase I)阶段。
原文链接:
https://jvi.asm.org/content/early/2020/04/09/JVI.00367-20.long
参考文献
1.Wang L, Chen X, Zhou X, Roizman B, Zhou GG.2018. miRNAs Targeting ICP4 and Delivered to Susceptible Cells in Exosomes Block HSV-1 Replication in a Dose-Dependent Manner. Mol Ther 26:1032-1039.
2.Runbin Yan, Xusha Zhou et al, Zhou G. 2019. Enhancement of oncolytic activity of oHSV expressing IL-12 and anti PD-1 antibody by concurrent administration of exosomes carrying CTLA-4 miRNA. Immunotherapy. Vol.5 Iss.1 No: 1000154.
3. Farnsworth A, Johnson DC.2006. Herpes simplex virus gE/gI must accumulate in the trans-Golgi network at early times and then redistribute to cell junctions to promote cell-cell spread. J Virol 80:3167-79.
4. Roizman B, Knipe DM, Whitley RJ. 2013. Herpes simplex viruses, p 1823-1897. In Knipe DM, Howley PM (ed), Fields' Virology, 6th ed. Wolters Kluwer/Lippincott-Williams and Wilkins, New York.
编者按:本文转载自微信公众号:生命科学前沿(ID:advancedlifesci),作者:周国瑛课题组
广告、内容合作请点这里:寻求合作
咨询·服务

